13162025768
免费试用
计算流体力学(CFD)在心血管系统中的应用是其在医学领域中最成熟、最深入的方向之一。它通过数值模拟血液流动的动力学特征如,流速、压力、剪切应力等,结合患者的影像数据重建个性化血管模型,为理解心血管疾病的发病机制、优化诊疗方案提供了量化依据。以下是其核心应用场景及解决的问题:
1、动脉粥样硬化的机制研究与风险预测
动脉粥样硬化是冠心病、脑梗死等疾病的核心病因,其斑块易在血管分叉、弯曲处,如颈动脉分叉、冠状动脉左前降支的形成,而血流动力学异常是关键诱因。
应用场景:
可解决的问题:
2、动脉瘤的生长与破裂风险评估
动脉瘤,如颅内动脉瘤、腹主动脉瘤,是血管壁局部膨出形成的“薄弱点”,其破裂可能导致致命性出血,而血流对瘤壁的力学作用是决定其生长和破裂的核心因素。
应用场景:
可解决的问题:
量化破裂风险:对未破裂动脉瘤,通过CFD参数区分“高风险”与“低风险”动脉瘤,避免过度治疗。
优化治疗方案:评估手术干预后的血流动力学变化,预测治疗效果,如是否有效降低瘤壁压力。
3、心脏瓣膜疾病的评估与人工瓣膜优化
心脏瓣膜的狭窄或反流会导致血流紊乱,而人工瓣膜的设计需平衡血流动力学性能与并发症风险。
应用场景:
4、先天性心脏病的血流动力学分析
先天性心脏病,如室间隔缺损、法洛四联症、主动脉缩窄等,会导致血流路径异常,引发心功能损害,而CFD可量化异常血流对心脏和血管的影响。
应用场景:
可解决的问题:
5、支架植入与血管重建的优化
冠心病、外周动脉疾病等需通过支架植入扩张狭窄血管,但术后可能出现再狭窄或支架血栓,血流动力学是关键影响因素。
应用场景:
可解决的问题:
6、心功能评估与心力衰竭机制研究
心力衰竭的核心是心脏泵血功能下降,而心室血流动力学与心肌收缩功能密切相关。
应用场景:
可解决的问题:
门静脉是肝脏的“物流总闸”,其位置如下图(a)所示。血流量占心输出量的25 %,却没有任何瓣膜;一旦血流动力学失衡,就可能引发门脉高压、血栓乃至肝性脑病。受制于伦理与成像极限,活体测量门静脉全域流速、壁面剪切应力(WSS)几乎不可能。
于是我们把血管“搬进”计算机,截取一段如下图(b)所示,用CFD让在血管内的行为变得可观测、可量化、可干预。
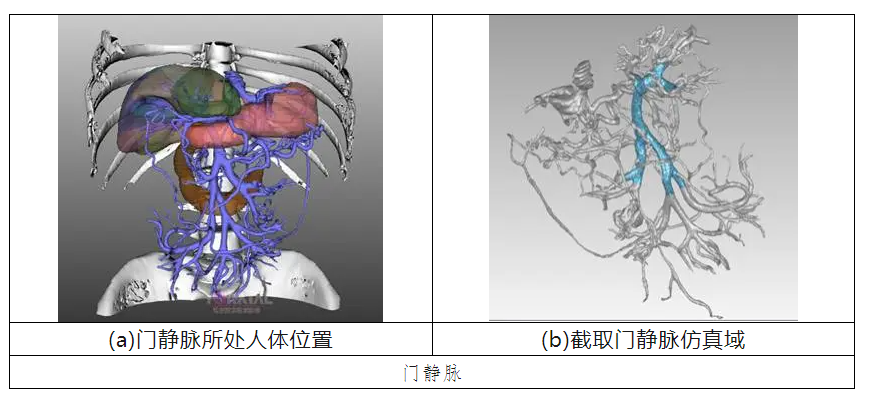
在此案例中,采用上海积鼎信息科技有限公司的自研CFD软件VirtualFlow 2025的非结构求解器进行仿真。该求解器支持任意的非结构网格,仿真精度不亚于主流上软,同时支持原生GPU计算,可大幅提升仿真速度。
a、CPU求解结果与主流商软对比
采用VirtualFlow进行网格划生成软件生成四面体网格,分别通过国外F软件和自研求解器用该网格进行仿真。从仿真的结果对比可以看出血管壁面上的压力分布基本一致,最大高压绝对值几乎一致,最低低压绝对值相差10%左右。
.png)
b、GPU求解结果与主流商软对比
积鼎科技VirtualFlow 2025版已支持GPU求解能力,其特色表现为:
1. 同时支持CPU和GPU计算
2. 支持任意多面体网格,适用于具有复杂几何外形的快速网格生成
3. 采用稳定高效的数值求解方法,可以求解多种流动特别是多相流问题
4. 支持定常和非定常求解
5. 支持多种湍流模型,包括但不限于k-epsilon、sst k-omega等
6. 具有全面的前后处理功能
7. 具有脚本功能,能够支持自动化运行
8. AI友好,可与AI模型连接
仿真结果对比
.png)
从上图的仿真结果比较来看,VirtualFlowGPU版与商软国外S软件的计算结果几乎一致,可见VirtualFlow GPU版本求解器数学模型的精度是可以信赖的。
仿真性能对标
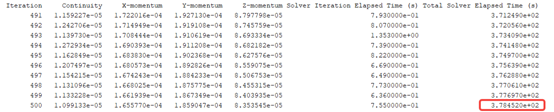
国外S软件核并行时间
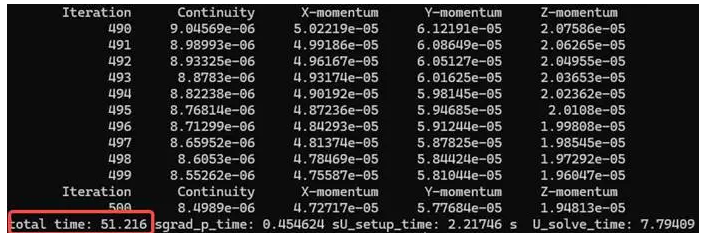
自研GPU版1卡并行时间
国外S软件在16核配置下仿真500步,耗时378s。相同的网格与模型配置下,采用VirtualFlow非结构求解器求解,在1块GPU显卡的情况下,同样计算500步,需要51s。可见自研非结构求解器的GPU版本计算效率是商软CPU计算的7~8倍。
c、与离散元软件DEMms耦合
在多物理场耦合数值方法及 CFD-DEM 单向耦合解析的基础上,针对红细胞与血流场的相互作用,虽正常生理状态下红细胞体积分数为 35%~50%,属于高浓度颗粒体系,二者相互作用具有强耦合特性,但为演示单向耦合,特设计如下测试算例。
该测试算例的核心是对红细胞相关参数进行特殊设定,以满足单向耦合的适用条件。在算例中,我们将红细胞的体积分数大幅降低至5% 以下,使其处于稀薄颗粒体系范畴。此时,可近似认为红细胞对血流场无显著扰动,仅需考虑血流场对红细胞的作用力,符合单向耦合 “上游计算结果驱动下游仿真,下游结果不反作用于上游” 的特征。
基于积鼎的颗粒流求解器DEMms,与非结构求解器耦合,实现红细胞在血管中流动的耦合仿真。通过下图耦合仿真结果可见,红细胞在中间交汇处容易聚集。通过耦合仿真,可以对血栓形成的研究体统理论依据。
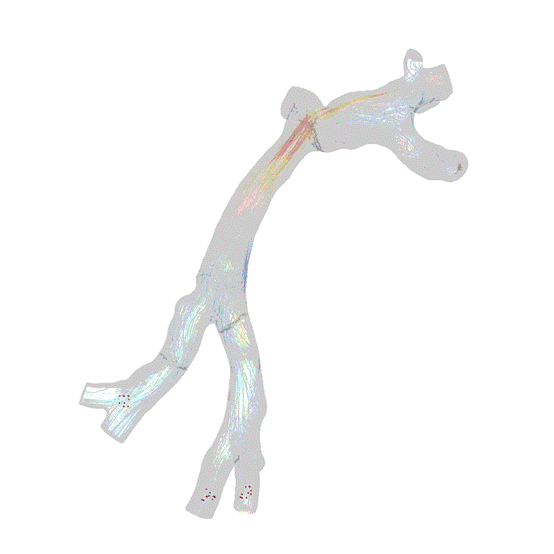
1. VirtualFlow2025版中的求解器可分结构模块求解器和非结构模块求解器。比于传统国外F软件等商软,只能提供一种模式,软件的仿真场景有更大适用性。
2. 同时支持CPU和GPU计算
a. GPU原生支持,性能不亚于国际主流GPU求解器
b. CPU支持多线程和多进程混合并行模式
c.同时适配国际主流和国内多种CPU/GPU
3. 支持任意多面体网格,适用于具有复杂几何外形的快速网格生成
4. 采用稳定高效的数值求解方法,可以求解多种流动特别是多相流问题
5. 支持定常和非定常求解
6. 支持多种湍流模型,包括但不限于k-epsilon、sst k-omega等
具有全面的前后处理功能
a. 高度自动化网格划分能力
b.高性能仿真结果后处理
7. 具有脚本功能,能够支持自动化运行
8. AI友好,可与AI模型连接
四、总结
CFD在心血管系统中的应用核心是将“形态学影像”转化为“力学量化指标”,解决了传统影像学无法回答的“力学机制”问题:
随着CFD技术与医学研究的结合,其在临床中的转化应用将更加广泛,推动心血管疾病诊疗从“定性描述”向“定量预测”发展。

官方微信

扫码关注